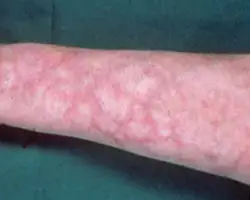
La sindrome da anticorpi antifosfolipidi è una sindrome particolare, il medico si imbatte molto facilmente e per questa ragione è bene analizzare tutti i suoi aspetti. Si caratterizza per la presenza di: 1) eventi trombotici che possono colpire sia vene che arteria in maniera ubiquitaria, e tra l’altro sono vasi usualmente non colpiti dall’aterosclerosi; 2)aborti ricorrenti; spesso proprio questa condizione permette la formulazione di una diagnosi in giovani donne che, avendo aborti ricorrenti, si rivolgono al medico e dopo una serie di indagini si scopre che la donna è affetta da sindrome da anticorpi antifosfolipidi; 3)livedo reticularis (in figura); 4) trombocitopenia; 5)presenza a livello sierico di autoanticorpi diretti contro fosfolipidi.
Gli anticorpi a cui si fa usualmente riferimento sono essenzialmente due: ACA (Ab anti cardiolipina) e LAC (lupus anti coagulant). In realtà in linea teorica, anche in linea pratica ma raramente, possono essere presenti ulteriori tipi di autoanticorpi diretti contro altri fosfolipidi, come per esempio gli anti fosfatidilserina, fosfatidilinositolo, fosfatidiletanolammina. In linea generale comunque i principali sono i primi due.
Quando parliamo di sindrome bisogna prima di tutto capire se questa sia una forma PRIMITIVA o SECONDARIA ad altre connettivopatie. La forma primitiva è quella in cui non si riescono a mettere in evidenza segni e sintomi o dati di laboratorio del Lupus Eritematoso Sistemico o altre patologie associate; la forma secondaria, invece, si instaura a causa di un’altra connettivite, in genere LES, ma può associarsi a AR, Sjögren, neoplasie (leucemia a cellule capellute), infezioni, farmaci; tra questi ultimi ricordiamo quei farmaci che possono interferire con la risposta immunitaria. Il nome del LAC potrebbe trarre in inganno per il termine “anticoagulant” potrebbe suggerire una reazione emorragica. In verità questo anticorpo in vitro da luogo ad una reazione di emolisi delle emazie, ma in vivo fa tutt’altro, cioè da luogo a fenomeni trombotici. Il LAC fu il primo individuato (da Conley e Hatman); anti cardiolipina invece è stato scoperto più di recente e circa 25 anni fa sono stati stilati i criteri per porre diagnosi.
Come per tutte le connettivi non si conosce un meccanismo eziopatogenetico, più che altro non se ne conosce l’etiologia; come sempre nell’ambito di queste malattie sistemiche esiste una certa predisposizione genetica , che si traduce in un’alterazione dei meccanismi di sorveglianza immunologica per cui si formano questi autoanticorpi non diretti esclusivamente verso un fosfolipide, ma verso complessi macromolecolari formati da proteine e fosfolipidi. Per quanto riguarda le proteine contro cui sono diretti questi anticorpi esse sono essenzialmente la β2 glicoproteina I e la protrombina
Il LAC in vitro interferisce con molti test della coagulazione che dipendano dalla presenza dai fosfolipidi, come il KTC (Tempo di Coagulazione al Caolino) , dRVVT (il test al Veleno di Vipera Russel diluito) e aPTT (Tempo di Tromboplastina Parziale Attivata). Questi test sono alterati e risultano allungati. Come abbiamo detto prima non abbiamo certezza su quale sia l’evento etiologico e non abbiamo certezze su cosa accada a livello patogenetico con precisione, ma è stato ipotizzato, secondo studi recenti, che ci possa essere un legame con il processo apoptotico,inserito in un contesto di predisposizione genetica; si è ipotizzato che durante l’apoptosi vengano esposti questi fosfolipidi capaci di suscitare una risposta immunitaria e quindi formazione di autoanticorpi. Quest’ultimi agiscono sulla coagulazione a diversi livelli:
1) sulla cascata della coagulazione;
2) a livello endoteliale;
3)sulle piastrine.
NELLO SPECIFICO:
-gli autoanticorpi interferiscono con la β2 glicoproteina I, che normalmente inibisce la cascata della coagulazione; di conseguenza non essendoci il “freno” proteico, poichè “attaccato” dagli autoanticorpi, l’attivazione della cascata della coagulazione sarà favorita con conseguente formazione di fenomeni trombotici.
-il danneggiamento dell’endotelio vasale; normalmente l’endotelio ha funzione antitrombotica grazie alla produzione di prostacicline che evitano l’adesione e quindi l’aggregazione delle piastrine e della loro attivazione. Se si verifica un danno a livello endoteliale avremo una minor produzione di prostacicline e l’adesione piastrinica sarà favorita così come l’evento trombotico per attivazione dei trombociti.
-gli autoanticorpi danneggiano anche le piastrine e ciò risulta un ulteriore stimolo all’attivazione di altri trombociti.
-alterazione funzione della PROTEINA C della cascata della coagulazione sempre in senso pro trombotico. Alterato rilascio di Acido arachidonico, con alterata formazione prostacicline e quindi marcata adesione.
Per quanto riguarda la clinica gli anticorpi antifosfolipidi inducono quindi:
-Trombosi venosa o arteriosa, che si può verificare in tutti i distretti, a livello di vasi di grosso, medio o piccolo calibro;la localizzazione è di solito preferenziale e imprevedibile, senza periodicità e fattore scatenante;
-Trombocitopenia, sia per un consumo di piastrine legato all’attivazione dei processi trombotici e sia da danneggiamento delle stesse;
-Poliabortività, dovuta ad una insufficienza placentare scatenata da eventi trombotici a questo livello;
A livello pratico possono verificarsi:
-eventi coronarici, infarto renale, livedo reticularis,neuropatie, trombosi delle arterie cerebrali con conseguente demenza multi-infartuale, crisi convulsive,corea.
-dal versante venoso possono verificarsi tromboflebite, embolia polmonare, sindrome di Budd-Chiari (frequentemente vengono colpite le vene).
-la livedo reticularis è una manifestazione particolare, e si appalesa come una rete rossastra soprattutto a livello degli arti. Ci possono essere altre manifestazioni a livello cutaneo come gangrena delle estremità, ischemia digitale, ulcere da stasi, necrosi superficiali. Naturalmente l’entità della manifestazione clinica è in relazione a quale distretto viene colpito, in quale misura e con quanta frequenza, perchè ad ogni modo gli eventi trombotici tendono a recidivare.
La presenza del LAC è associata a un maggior rischio di eventi trombotici rispetto alla presenza dell’anticardiolipina; anche l’anticardiolipina si associa a rischio trombotico ma a titoli anticorpali più elevati, e naturalmente se viene refertato un titolo elevato di questo anticorpo bisogna accertarsi che non sia legato a infezioni o farmaci, e in quest’ultima evenienza il rischio di trombosi è meno elevato.
Abbiamo poi visto che un altro segno importante nella patologia in esame è la trombocitopenia che è legata maggiormente ad un consumo di piastrine e attivazione.qualche volta, fortunatamente è un’evenienza rara, si può verificare una sindrome da Occlusione Catastrofica che si caratterizza per occlusioni vascolari ad interessamento multiorgano. Frequentemente la diagnosi si effettua in donne giovani con poliabortività, e quindi qual’ora si presenti una giovane donna con problema di aborti ricorrenti si valuta in generale (e si deve valutare) l’evenienza di una sindrome da anticorpi antifosfolipidi. La diagnosi viene fatta se viene soddisfatto almeno 1 criterio clinico e 1 laboratorio.
CRITERI CLINICI:
-Trombosi vascolare; almeno 1 o + eventi di trombosi vascolare venosa o arteriosa.
-Poliabortività. BISOGNA CAPIRE IL TIPO DI ABORTO: 1) morte fetale intrauterina dopo la 10^ settimana di gestazione con normale morfologia del feto,documentabile o con ecografia o con osservazione diretta; 2) una o + nascite premature di neonati morfologicamente normali alla 34^settimana o prima 3) 3 o + morti fetali inspiegabili,consecutive,entro la 10ì sett. Escludendo cause ormonali, anomalie morfologiche e genetiche.
CRITERI DI LABORATORIO:
-Positività per anticardiolipina.
-Positività LAC.
Non basta misurarli una sola volta; bisogna misurarli su 2 campioni diversi di siero prelevati almeno con un intervallo di 6 settimane. Per essere confermato, il criterio deve esplicarsi in entrambi i prelevi. La diagnosi può essere fatta solo se presente un criterio clinico e uno di laboratorio.
TERAPIA: utilizzo di antiaggreganti e anticoagulanti.
ASPIRINA:<antiaggregante> relativamente sicuro come farmaco ma con effetti limitanti e può essere assunto da soggetti con forme più lievi. Warfarin (anticoagulante) è il farmaco d’elezione, ma se la paziente è una donna in gravidanza non può essere usato visto l’effetto teratogeno e in questi casi si fa assumere l’eparina. In ACUTO bisogna immediatamente scoagulare con eparina e.v. che ha un effetto immediato e poi Warfarin per os. Questo nelle forme primitive.Nelle forme secondarie invece bisogna prima di tutto trattare la patologia sistemica di base.
Analizziamo ora il metabolismo CALCIO/FOSFORO E OSTEOPOROSI. Il mantenimento della calcemia è fondamentale perchè il livello del calcio intra- ed extracellulare regola molti processi cellulari.Di tutto il Calcio presente nel nostro organismo la stragrande maggioranza è presente nelle ossa, il 98% per la precisione è presente nelle ossa, si tratta di un pool stabile (nel senso che difficilmente viene scambiato) e di un pool instabile (meno dell’1% una piccola parte che viene scambiata). Del restante 2 % sul totale abbiamo per metà il calcio plasmatico e l’altra metà il calcio intra ed extracellulare. Il Calcio che si trova nel plasma è l’1% del calcio totale, di cui metà è libero cioè ionizzato cioè quello metabolicamente attivo, quello che realmente serve alle cellule; un’altra metà è legato a proteine ; tra le proteine l’albumina è la principale. La quantità di calcio è legata strettamente alla quantità di albumine sieriche, e quindi per sapere con precisione qual è il calcio attivo dobbiamo operare delle correzioni in base al livello di albumina.Questo perchè a noi interessa la quantità di calcio circolante con precisione. La correzione viene effettuata considerando che l’Albuminemia normale è considerata 4,1; per ogni grammo di albumina in più o in meno bisogna togliere o aggiungere 0,8 mg di calcio.
Calcemia totale (mg/dl) Albuminemia Calcemia “corretta” (mg/dl)
8,5 3,1 9,3
10,3 5,1 9,5
Ogni giorno mangiamo circa 1000 mg di calcio, di cui 800 mg vengono persi con le feci e 200 mg vengono riassorbiti a livello intestinale; a livello renale ne vengono escreti circa 200mg e di conseguenza il bilancio tra assorbimento intestinale ed escrezione renale è in pareggio. Una quantità esigua inoltre viene scambiata giornalmente con il pool labile osseo. A livello renale la maggior parte del calcio filtrato viene riassorbito e una piccola quota viene escreta.
Il calcio viene riassorbito essenzialmente o per trasporto attivo o per trasporto passivo. Il trasporto attivo utilizza dei trasportatori del calcio ad attività ATPasica, saturabili e dipendenti fortemente dalla concentrazione di vitamina D. Il trasporto passivo sfrutta il gradiente osmotico e dipende dalle conc intestinali di calcio essenzialmente e non va incontro a saturazione; di conseguenza se vogliamo aumentare il riassorbimento di calcio dobbiamo farne assumere una quantità maggiore attraverso, per esempio i supplementi, in modo che oltre al trasporto attivo venga utilizzato il trasporto passivo!
In condizioni fisiologiche il nostro organismo riesce con il trasporto attivo e vitamine a determinare la quantità di calcio da assorbire. Ad esempio con un apporto di calcio nella dieta di 800 mg(apporto basso) il calcio assorbito sarà 200 mg tutto per trasporto ATTIVO ossia il 25% dell’apporto e per fare questo c’è maggior bisogno di vitamina D per attivare tutti i trasportatori. Se l’apporto sarà di mille sempre 200 mg sarà il calcio riassorbito cioè il 20 %.Se l’apporto è di 1200(elevato) il calcio assorbito sarà sempre di 200 mg mediante trasporto attivo cioè il 17% con un minore utilizzo di vitamina D. Da qui possiamo ben capire che il trasporto attivo è saturabile, ed ecco il motivo per cui nonostante una quota importante di calcio, 1200mg,il calcio riassorbito sarà sempre di 200 mg.
Il trasporto attivo si realizza a livello del piccolo intestino; nella parte terminale, ovvero a livello dell’ileo,si realizzano i meccanismi di trasporto passivo calcio-dipendente. In una dieta normale con apporto di 1gr, abbiamo visto che 200mg vengo riassorbiti attivamente, ma la quantità residua che giunge all’ileo è talmente bassa da non permette il riassorbimento passivo. Al contrario in una dieta ricca di calcio, per es con assunzione cospicua di 1,2 gr a livello dell’ileo giungerà una quantità “utile” affinchè possa realizzarsi il trasporto passivo.
RELAZIONE CALCOLOSI RENALE-ASSUNZIONE ELEVATE QUANTITA’ DI CALCIO: Si è sempre pensato che mangiare molto calcio potrebbe causare problemi di calcolosi renale. In realtà dal grafico si evince che più calcio c’è nella dieta più il rischio di calcolosi si riduce! Per quale motivo: perché se aumenta il calcio nella dieta in modo naturale, succede che 200 mg vengono assorbiti per trasporto attivo e un poco ne rimane e giunge fino all’ileo dove il calcio inibisce il riassorbimento di ossalati, importanti per la formazione di calcoli! Mentre chi assume supplementi di calcio (integratori farmacologici) il rischio effettivamente aumenta, ma di poco. Perché la quantità di calcio che arriva all’ileo è così abbondante che aumenta la calciuria e quindi aumenta la probabilità di calcoli renali.
Come viene eliminato il calcio? Essenzialmente per via fecale e 200mg circa per via renale, che sono poi quei 200mg che dobbiamo recuperare con la dieta. Una quota piccolissima anche attraverso il sudore viene eliminata.
FABBISOGNO DI CALCIO, varia in base ad età e sesso:
Gruppo di età Anni mg/die
Neonati/bambini 0-10 400-1200
Adolescenti/giovani adulti 10-20 1200-1500
Donne Pre-menopausa 1000
Gravidanza/allattamento 1200-1500
Oltre 65 1500
Uomini 25-65 1000
Oltre 65 1500
Negli ultimi tempi è stato effettuato uno studio presso il comune di Brisighella e si è visto come rispetto ai dati teorici relativi alle quantità consigliate di calcio da assumere giornalmente, in effetti se ne assume una quantità sensibilmente inferiore, soprattutto nei soggetti con età superiore ai 65 anni. Naturalmente questo studio esemplifica ciò che avviene più o meno in tutta l’Italia. Ruolo del PTH il suo rilascio è stimolato dalle basse concentrazioni di calcio ematico e in netta risposta le paratiroidi rilasciano il PTH. Nel caso in cui abbiamo un basso introito di calcio ( < 500 mg/ die) cosa succede? diminuisce il calcio sierico → aumenta in maniera consistente il PTH che fa le stesse cose dette prima (aumenta la sintesi di vitamina D e aumenta l’escrezione di fosfati) ma in più, essendo così alto, avviene un bilancio negativo di calcio a livello dell’osso. Se lo stimolo prosegue poichè si continua a non assumere adeguate dosi di Calcio, la continua secrezione di PTH si può tradurre in un IPERPARATIROIDISMO e indurre un bilancio negativo dell’osso che depaupera. L’aumento del PTH può verificarsi in acuto ( viene rilasciato il PTH preformato e contenuto in granuli all’interno delle cellule della paratiroide) o in cronico (lo stimolo continuo induce un riarrangiamento dei geni che codificano la produzione del PTH e di conseguenza aumenterà cronicamente la sua produzione).
Effetto del PTH a livello osseo: Il PTH causa l’assorbimento del calcio per attivazione degli osteoclasti; il PTH favorisce la differenziazione da precursore dell’osteoclasta in osteoclasta maturo. Il precursore per diventare maturo ha necessità che un recettore presente sulla sua superficie, recettore RANK, venga legato dal RANK-LIGANDO presente sugli osteoblasti; ma è anche necessario che ci sia l’intervento di un fattore di crescita l’MCSF; il PTH stimola la produzione di questo MCSF e stimola la produzione di RANK-L, ma inibisce anche la produzione della proteina OSTEOPROTEGERINA che blocca il RANK-L. così tutto queste azioni fanno si che si produce RANK-Ligando che induce la trasformazione del precursore degli osteoclasti in osteoclasti maturi che riassorbono tessuto osseo mettendo in circolo il calcio e depauperando l’osso. Il PTH è un ormone interessante che viene utilizzato anche nella terapia dell’osteoporosi, uno potrebbe dire, come il PTH attiva gli osteoclasti e io lo uso per curare l’osteoporosi? Si, perché l’azione del PTH varia a seconda che l’esposizione del tessuto osseo sia continua o discontinua. Se il tessuto osseo è costantemente esposto ad una grossa quantità di PTH, gli osteoclasti sono molto attivati, gli osteoblasti lo sono un po’ meno. Ma se l’esposizione dura solo un’ora al giorno gli osteoblasti sono attivati moltissimo, gli osteoclasti sono attivati quasi per nulla. Questo è il motivo per cui oggi nella terapia dell’osteoporosi si utilizza anche il PTH, perché quando diamo il PTH ed esponiamo l’organismo al PTH per poco tempo, questo PTH induce attivazione degli osteoblasti e una scarsa attivazione degli osteoclasti.
VITAMINA D àLa vitamina D viene sintetizzata a partire dalla cute a partire dal 7-deidrocolesteorlo che ha il nucleo del ciclo pentano peridrofenantrene sotto l’azione dei raggi ultravioletti (UVB in particolare) si ha la formazione prima della pre-vitamina D3 e poi grazie al calore corporeo la formazione della vitamina D3. Viene sintetizzata quasi sempre, nei mesi estivi alle nostre latitudini se ne produce di più, quindi non dipende solo dal tempo di esposizione ma anche dall’intensità dei raggi che colpiscono la cute. Se andiamo a vedere cosa accade negli anziani, notiamo che gli anziani sono molto meno efficienti nel produrre vitamina D rispetto ai giovani, altro motivo per cui il fabbisogno di calcio aumenta con l’età!La vitamina D viene prodotta solo dalle cute ma si trova anche negli alimenti come l’olio di fegato di merluzzo che è ricchissimo di vitamina D rispetto ad altri alimenti come le uova o il latte . L’80% del fabbisogno di vitamina D è garantito dall’esposizione al sole.
A livello renale c’è l’enzima 1-alfa-deidrossilasi che serve appunto per idrossilare la vitamina D quindi chi ha insufficienza renale avrà problemi con l’idrossilazione della vitamina D, questo succede solo quando l’insufficiente è importante, con una creatinemia che supera 1,7 – 1,8 , mentre per insufficienze moderate non ci sono modificazioni sull’enzima. Se produco poco vitamina (poca esposizione solare ad esempio o perché non la introduco con gli alimenti) c’è un rapporto tra vitamina D (25-OH-vitamina D forma di deposito ) e PTH: quando diminuiscono le forme di vitamina D in deposito aumenta il PTH, quindi un’ipovitaminosi D può causare un iperparatiroidismo secondario che è compensatorio ovviamente per tenere normale i livelli di calcio. Oggi, se la quantità di vitamina D si riduce sotto i 20 (credo intenda nanogrammi) si può andare incontro a iperparatiroidismo secondario. I valori normali di vit D sono maggiori di 30 ng / ml ( o 70-90 nmol/l).
La carenza di vitamina D si espleta già per valori inferiori ai 30 ng/ml come forma severa e prolungata(osteomalacia); carenza non severa ma prolungata (diminuzione dell’assorbimento intestinale di calcio con diminuzione della calcemia e aumento del PTH, aumento del riassorbimento osseo fino adosteoporosi e fratture); come miopatia prossimale con disturbi dell’equilibrio con aumento del rischio di fratture.