L’empiema è una raccolta di pus in una cavità preformata (pleura, peritoneo, colecisti ecc).
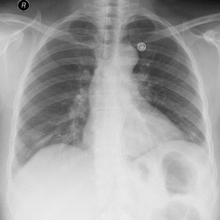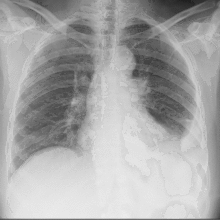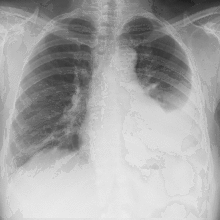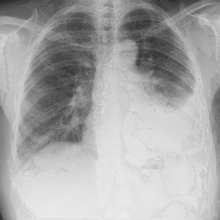
La patogenesi dell’empiema pleurico
La patogenesi dell’empiema pleurico riconosce tre differenti situazioni:
– contaminazione da una sede contigua allo spazio pleurico (50-60%): polmone, mediastino (esofago e linfonodi), collo, parete toracica, colonna vertebrale, cavità peritoneale;
– inoculazione diretta nello spazio pleurico (30-40%): procedure diagnostiche invasive (ad esempio un agoaspirato percutaneo effettuato per recuperare elementi cellulari da un addensamento polmonare), infezioni postoperatorie, ferite toraciche penetranti;
– infezione ematogena dello spazio pleurico (1%): è un’evenienza abbastanza rara.
Pleurite
Una polmonite che interessa un lobo, un segmento o le porzioni più peri-bronchiali non crea molti danni. Se, invece, essa interessa la superficie pleurica del polmone, può svilupparsi una pleurite consensuale della viscerale, che, poi, dissemina nello spazio pleurico (pleuropolmonite). Dunque, si forma un versamento “meta-pneumonitico”.
L’empiema metapneumonico rappresenta il 50% di tutti gli empiemi. Il 40% di tutti i pazienti con polmonite batterica ha anche un versamento pleurico associato, che può trasformarsi in un empiema.
Fattori predisponenti all’empiema:
– alcolismo;
– epatopatia;
– malattie polmonari croniche;
– diabete;
– TBC inattiva;
– terapia steroidea;
– abuso di sostanze stupefacenti.
Quadro clinico dell’empiema:
Il quadro clinico è caratterizzato da:
– segni e sintomi di infezione generalizzata: febbre, sudorazione notturna;
– segni e sintomi toracici : dolore toracico, tosse, dispnea;
A volte il quadro clinico è difficilmente distinguibile dalla sintomatologia relativa alla patologia polmonare di base.
Gli empiemi da microrganismi aerobi hanno, solitamente, un decorso acuto, a volte con sepsi. Gli empiemi da anaerobi hanno un decorso più subdolo, perché sono più difficilmente identificabili dal sistema immunitario e la loro azione si esplica soprattutto con la dismissione di endotossine, che possono essere molto pericolose. Invece, gli aerobi evocano una reattività maggiore da parte dell’organismo.
Prima dell’era antibiotica, il germe più coinvolto era Streptococcus pneumoniae. Negli anni ’60, era frequentissimo l’empiema da Staphilococcus aureus. Dagli anni ’70 in poi, sono aumentati gli empiemi sostenuti da batteri anaerobi o, addirittura, di natura polimicrobica.
Su cosa si basa la diagnosi dell’empiema:
La diagnosi si basa su:
– quadro clinico;
– aumento degli indici di flogosi (VES e PCR), ricordando che per seguire un’infezione bisogna preferire la PCR, dato che è molto più sensibile (valore massimo normale = 0,5). La VES può normalizzarsi anche a distanza di 6 mesi dall’infezione;
– Rx torace;
– TC torace;
– prelievo di materiale purulento dal cavo pleurico, precisando che nella maggior parte dei casi la sua utilità è limitata dal fatto che l’esame colturale si rivela negativo, a causa del trattamento antibiotico somministrato al paziente.
I vari stadi dell’empiema:
Nell’empiema si individuano tre stadi:
Stadio I o fase essudativa
si verificano un ispessimento delle membrane pleuriche e la produzione di liquido di tipo essudativo, per aumento della permeabilità della pleura viscerale. Un tempo si effettuava la prova di Rivalta per stabilire se il liquido in esame era di tipo essudativo o trasudativo. Essa si basava sul fatto che nel liquido essudativo è presente una certa quota di proteine (assente in quello trasudativo), che produce una caratteristica “nubecola”, se posto in una soluzione contenente acido acetico. Oggi questa prova non viene più effettuata. In questa fase il liquido è ancora chiaro e rappresenta la risposta della pleura all’insulto infettivo.
Stadio II o fase fibrino purulenta
Questa fase inizia la deposizione di fibrina e si formano delle concamerazioni. L’organismo cerca di difendersi, circoscrivendo e limitando il danno.
Stadio III o fase di organizzazione
In questa III fase c’è una produzione di collagene da parte di fibroblasti, che cercano di murare la lesione.
Dal punto di vista diagnostico, si ha la possibilità di seguire questi stadi con la TAC e con l’ecografia. Questa stadiazione è valida per tutti gli empiemi, non solo per quello metapneumonico.
Trattamento dell’empiema
Il trattamento varia a seconda dello stadio dell’empiema.
Trattamento nel I stadio dell’empiema:
Nel primo stadio, esso consiste nella terapia antibiotica e nel drenaggio. Evacuando tutto il liquido contenuto nella cavità pleurica, si favorisce l’espansione polmonare, che è la migliore cura per la polmonite sottostante. Le polmoniti guariscono spontaneamente, a patto che il polmone sia ben ventilato e che le secrezioni vengano allontanate con l’espettorazione. Se c’è un versamento pleurico associato, la cosa migliore da fare è evacuare il liquido perché, da una parte si riduce la carica batterica, dall’altra si favorisce l’espansione del polmone. Nel primo stadio, il liquido è distribuito in una sola cavità, non ci sono concamerazioni. Dunque, attraverso un drenaggio, è possibile evacuarlo completamente.
Trattamento nel II stadio dell’empiema:
Nel secondo stadio, il trattamento consiste nel continuare la terapia antibiotica e il drenaggio. Inoltre, è possibile somministrare, attraverso il drenaggio toracico, delle sostanze fibrinolitiche, che, però, sono particolarmente costose e non vengono quasi mai utilizzate. Nel secondo stadio, il drenaggio ha il limite di non permettere l’evacuazione completa del liquido, per l’impossibilità di accedere a tutte le concamerazioni.
Dunque, è necessario ricorrere alla toracoscopia. Il paziente viene portato in sala operatoria e viene intubato con un tubo a doppio lume, che esclude dalla ventilazione il polmone sul quale si opera. Il polmone escluso, se non ha aderenze, si affloscia progressivamente, ottenendo uno spazio utile per l’operazione. Nella toracoscopia si effettuano dei piccoli accessi, si introduce l’ottica e con degli strumenti si rompono le concamerazioni per portar via tutta la fibrina.
Trattamento nel III stadio dell’empiema:
Nel terzo stadio la pleura si ispessisce a tal punto da diventare una cotenna, che impedisce la ventilazione intrappolando il polmone. La mancata ventilazione non fa altro che mantenere il quadro infettivo. In questo caso, il trattamento non è toracoscopico, ma consiste in un approccio chirurgico a cielo aperto, che permette di asportare pleura viscerale e parietale, non totalmente, ma in corrispondenza della “sacca empiematosa”, con la successiva formazione di aderenze fra il polmone e la parete toracica. Questo tipo di intervento riguarda più frequentemente le parti basse del torace, piuttosto che quelle poste in alto.

