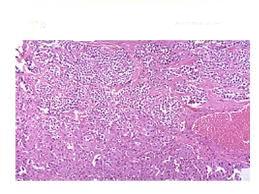
Nella sindrome mielodisplastica la differenziazione terminale è osservata, ma è alterata, nella leucemia acuta è bloccata e si avranno un pool di cellule nella fase precoce dell’ematopoiesi. Nella leucemie acute il commitment è bloccato mentre nelle sindrome mielodisplastiche c’è, ma è fortemente alterato.
Le tipiche anomalie morfologiche della sindrome mielodisplastica sono:
Asincronismi maturativi: cioè il nucleo e il citoplasma non maturano nello stesso modo;
Ponti citoplasmatici tra cellule che non si sono divise e rimangono attaccate mediante una porzione di membrana;
Alterazioni del numero e della forma dei nuclei dei megacariociti e dei granulociti;
Ipogranulosità nei neutrofili mature.
Classificazione:
Anemie refrattarie con eccesso di blasti;
Si ha un alto numero di blasti con conseguente difficoltà delle cellule a differenziarsi, essendo cellule della fase precoce dell’ematopoiesi.
– Normalmente il numero di blasti è inferiore o uguale al 5% della cellularità totale;
– Se il valore è compreso tra 5% e il 20% si è nel contesto di sindromi mielodisplastiche:
– in particolare, si avrà una sindrome mielodisplastica del tipo citopenia refrattaria con eccesso di blasti di tipo 1 se il valore è compreso tra il 5% e il 10% e
– di tipo 2 se il valore è compreso tra il 10% e il 19%,
– mentre dal 20% in poi si avrà una leucemia acuta.
Altre forme:
– non classificabili;
– isolata delezione del cromosoma 5q;
– variante childhood.
Clinica: La mielodisplasia in genere non è accompagnata da particolari problemi clinici, a meno che non ci sia una grave piastrinopenia con emorragie ricorrenti o una leucopenia che causa al paziente infezioni ricorrenti. Comunemente il paziente presenta anemia che va sempre indagata, come la piastrinopenia.
Diagnosi: il processo diagnostico del MDS consiste nel prelievo del midollo osseo (aspirato midollare), grazie al quale è possibile evidenziare la morfologia delle linee ematopoietiche, quindi se sono presenti alterazioni morfologiche o meno e di quantificarle in percentuale. Per terminare la diagnosi vi è bisogno anche delle anomalie citogenetiche. Esistono delle anomalie citogenetiche come la delezione del Cromosoma Y o del Cromosoma 1 (braccio q) che hanno una prognosi molto buona (sopravvivenza di 5 anni). Mentre nel caso di monosomia del Cromosoma 7, delezione del Cromosoma 7, Cariotipo Complesso (con più di tre anomalie) la prognosi è particolarmente infausta (sopravvivenza di 7 mesi). Dalla complessità citogenetica dipende il tempo di evoluzione verso la Leucemia Acuta: questo tempo non è definito per le forme a buona prognosi mentre non si supera l’anno per un cariotipo complesso (complessità citogenetica).
Prognosi: Le sindromi mielodisplastiche si distinguono in due forme:
de novo: il paziente non aveva nessuna patologia di tipo oncologico ma l’ha sviluppata in seguito alla displasia; rappresentano oltre l’85% di tutte le forme. Le forme secondarie possono essere: – Generalmente iatrogene: dipendenti da una radioterapia per malattie oncologiche o oncoematologiche;
– Esposizione ad agenti responsabili anche di leucemia acuta (come i pesticidi).
secondarie: dovute a trattamenti (come radio o chemioterapia) di altre patologie oncologiche, sia solide che ematologiche, che oltre all’azione terapeutica hanno provocato un danno al midollo e una serie di mutazioni che a loro volta hanno alterato la differenziazione e determinato la prevalenza di un clone o una serie di cloni. Le secondarie, quindi, sono causate da mutazioni indotte dal trattamento, non accumulate con l’età come nelle de novo, il che rende il processo più aggressivo rispetto ad un processo naturale e di conseguenza con una prognosi peggiore, così come le leucemie secondarie sono considerate peggiori.
Terapia:
- Per le forme a buona prognosi Tendenzialmente non si dà un trattamento se non terapie di supporto che nello specifico sono fattori di crescita, di solito l’eritropoietina con o senza il G-CSF.
- Gruppo a prognosi peggiore, che in realtà si distingue in: a prognosi intermedia;a cattiva prognosi. 5 AZA citidina.
- Il trapianto allogenico, ma è difficile da realizzarsi perché si tratta in genere di pazienti anziani, in una fascia d’età di solito di 65 anni, in cui difficilmente è possibile eseguire un trattamento che comprende il trapianto, anche se risolutivo. I bambini solitamente si indirizzano direttamente al trapianto, a cui segue la guarigione.